6.2.2 凝縮曲線の作り方
凝縮曲線、すなわちコンデンシング・カーブ(condensing curve)は混相状態における熱交換器の設計に不可欠な物性の一つで、その中に含まれている情報は、
- 熱交換器入口および出口における気液比(モル比あるいは重量比)と組成、ならびに気液それぞれの物性(密度または分子量、比熱、熱伝導率、粘度)
- 熱交換器入口~出口までの分割された区間における気液比(モル比あるいは重量比)と組成、ならびに気液それぞれの物性(密度または分子量、比熱、熱伝導率、粘度)
- 熱交換器入口~出口間での凝縮または蒸発の開始温度(露点または沸点)
- 熱交換器入口~出口間での気液それぞれの熱量と、入口と出口の熱量差(すなわち交換熱量)
単相における熱交換器と異なり、伝熱現象が異なるために多くの情報を必要とします。
この凝縮曲線を作成するためには、入口~出口までの分割された区間における各物質の蒸気圧が必要となります。ここでは説明を簡単にするために対象とする流体を空気とスチームの混合気体とします。その入口出口における流量や組成およびスチームの蒸気圧、そしてエンタルピを下記に示します。(エンタルピは25℃基準としています)
なお、圧力(全圧)は1.0MPaで空気流量および水蒸気+水流量はそれぞれ1000kmol/hとします。また、各温度における水蒸気流量は次式から計算しています。
水蒸気流量 = 空気流量×蒸気圧/(全圧-蒸気圧)
| 温度 | 蒸気圧 | 水蒸気 | 水 | 水蒸気 | 水 | 水蒸気+水 | 空気 |
| deg.C | MPa | エンタルピ kJ/kg | 流量 kmol/hr | ||||
| 0 | 0.0006 | 2396.1 | -104.9 | 0.6 | 999.4 | 1000.0 | 1000.0 |
| 20 | 0.0023 | 2432.6 | -20.9 | 2.3 | 997.7 | 1000.0 | 1000.0 |
| 40 | 0.0074 | 2468.7 | 62.7 | 7.4 | 992.6 | 1000.0 | 1000.0 |
| 60 | 0.0199 | 2504.0 | 146.3 | 20.4 | 979.6 | 1000.0 | 1000.0 |
| 80 | 0.0474 | 2538.2 | 230.1 | 49.8 | 950.2 | 1000.0 | 1000.0 |
| 100 | 0.1014 | 2570.7 | 314.3 | 112.9 | 887.1 | 1000.0 | 1000.0 |
| 120 | 0.1987 | 2601.1 | 398.9 | 247.9 | 752.1 | 1000.0 | 1000.0 |
| 140 | 0.3615 | 2628.6 | 484.4 | 566.2 | 433.8 | 1000.0 | 1000.0 |
| 150 | 0.4761 | 2641.1 | 527.4 | 908.8 | 91.2 | 1000.0 | 1000.0 |
| 160 | 0.6181 | 2662.5 | 570.7 | 1000.0 | 0.0 | 1000.0 | 1000.0 |
| 180 | 1.0026 | 2707.6 | 658.3 | 1000.0 | 0.0 | 1000.0 | 1000.0 |
| 200 | 1.5547 | 2751.1 | 747.6 | 1000.0 | 0.0 | 1000.0 | 1000.0 |
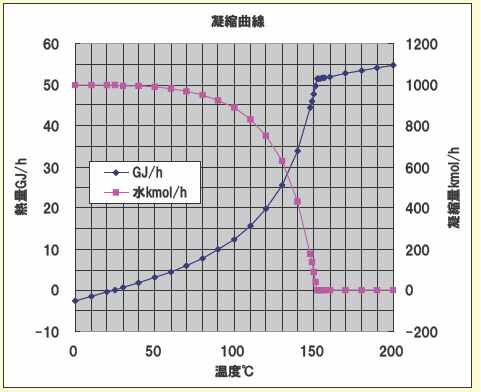
この表から水蒸気および水のエンタルピと流量を掛けて熱量を計算します。さらに空気のエンタルピ(kJ/kg or kJ/kmol)を求め、同じく空気の熱量を計算します。次に先ほどの水蒸気と水の熱量を合計し、横軸に温度をとってプロットすれば凝縮曲線を求めることができます。その結果を下図に示しました。また、横軸に温度、縦軸に水の流量をプロットすれば凝縮量の推移を見ることが出来ます。
熱量 = 水蒸気流量×水蒸気エンタルピ+水流量×水エンタルピ+空気流量×空気エンタルピ
なお、露点付近(150℃)では温度区間を細かくすることにより、凝縮曲線の変化が良くわかるようになります。
- 第1章 物質収支の計算
- 1.1 設計基本
- 1.2 物質収支計算ツールの準備
- 1.3 原子バランスの組み込み
- 1.4 気液分離
- 1.5 ストリームの合流(Addstream)
- 1.6 平衡定数の計算
- 1.7 平衡定数近似式の確定
- 1.8 平衡定数Kと圧平衡定数Kp
- 1.9 水蒸気改質炉出口組成計算
- 1.10 凝縮水分離とPSA水素精製
- 1.11 改質条件とCO転化条件と水素回収率への影響
- 第2章 熱収支の計算
- 2.1 熱収支計算の基礎
- 2.2 熱収支計算表の作成
- 2.3 ガス系の加熱と冷却
- 2.4 水蒸気改質炉の物質熱収支
- 2.5 予熱空気と水蒸気改質炉
- 2.6 燃焼系熱回収とスチーム発生
- 2.7 改質炉対流部プロセス設計
- 第3章 容器の設計
- 3.1 容器の種類
- 3.2 貯蔵タンク
- 3.3 分離器
- 第4章 回転機の設計
- 4.1 回転機の基礎
- 4.2 ポンプの設計
- 4.2.1 ポンプの種類と選定
- 4.2.2 ポンプのデータシート
- 4.2.2 ポンプのデータシート(流量について)
- 4.2.2 ポンプのデータシート(揚程について)
- 4.3 遠心ポンプの設計
- 4.3.1 遠心ポンプ効率の推定
- 4.3.2 遠心ポンプのNPSH
- 4.3.3 遠心ポンプのプロセス計算
- 第5章 水蒸気改質炉設計
- 5.1 改質管の設計
- 5.1.1 改質管とは
- 5.1.2 改質管の材料
- 5.1.3 Larson-Miller Parameter(LMP)
- 5.1.4 改質管の肉厚計算
- 5.2 水蒸気改質炉対流部の設計
- 5.2.1 伝熱計算
- 5.2.2 スタートアップ時の挙動
- 5.3 運転停止と水蒸気改質炉の設計
- 5.3.1 運転停止の種類
- 5.3.2 緊急停止における水蒸気改質炉
- 5.3.3 対流部熱交換器のクリープ破断
- 5.4 安全停止と改質炉設計
- 第6章 熱交換器の設計
- 6.1 熱交換器とプロセス設計
- 6.1.1 熱交換器性能とその影響
- 6.1.2 熱交換器のプロセスデータ
- 6.2 熱交換器と物性
- 6.2.1 凝縮と物性
- 6.2.2 凝縮曲線の作り方
- 6.2.3 凝縮曲線と熱交換器設計
- 6.2.4 エンタルピーの計算
- 6.2.5 凝縮熱伝達と有機溶剤
- 6.2.6 凝縮熱伝達と不凝縮ガスの影響
- 6.2.7 熱伝達と粘度の影響
- 6.2.8 熱伝達と材料の影響
- 6.3 熱交換器の選定
- 6.3.1 熱交換器の分類と種類
- 6.3.2 シェルとチューブ
- 6.3.3 熱交換器の用途とTEMA型式
- 第7章 計装制御
- 4.1 FLPT
- 4.2 圧力制御
- 4.2.1 化学プラントにおける圧力制御
- 4.2.2 圧縮機吸込側の圧力制御システム
- 4.2.3 圧縮機吸込側の圧力調節弁の容量
- 4.2.4 圧力上昇の要因
- 4.2.5 Closed outlet



 前のページへ
前のページへ