|
アンモニアプロセス
アンモニアはエチレンやメタノールと同じく主要な化学基礎原料で、世界のアンモニア需要は2011年で1億2千万トン、2011年以降も3.2%の伸び率を示し、2020年には1億6千万トンを超える規模になると予測されています。
アンモニアの最大の用途は肥料用尿素の原料です。国連などの統計によれば、人口の伸び率1%強に対し肥料の伸びが3倍以上の3.2%になっています。その背景には耕地面積の伸び率が0.06%と少ないため、単位面積当たりの穀物の収率増大を図らなければならないこと、生活レベルの向上による1人当たりの食物消費量の増大があるようです。そのために2015年以降に推測されるアンモニアの需要の伸びは年間で4百万トン強、年産7十万トンのプラントであれば1年間で6基づつ建設する必要があります。また、同じくアンモニアを原料に製造される硝酸は爆薬の原料に使用されています。
多くのアンモニアプラントは、水素およびメタノールプラントと同様に天然ガスを改質して得られる水素と空気中の窒素から製造されます。 アンモニアプロセスの歴史 18世紀以降の産業革命とそれがもたらした人口爆発に伴う食糧危機、それを補うための肥料の三大要素の一つである窒素の供給源(一例を挙げると尿素)としてアンモニア合成は科学界から期待されていました。
その当時、ドイツの化学会社BASFはノルウェー水力発電とともに電弧法によるアンモニア製造会社を作っていましたが、経済的には成立しませんでした。そこでハーバーのアンモニアの直接製造法に着目し、その工業化に会社の未来を託しました。それを主導した化学者のフリッツ・ボッシュとドイツBASF社のエンジニアのカール・ボッシュは後年ノーベル賞を得ており、このアンモニアの合成を成功させたBASF社は現在に至るまで世界屈指の総合化学会社で有り続けています。
ハーバー・ボッシュ法アンモニア合成の開発過程で大きな障害となったのが、触媒の開発と水素の製造、そして合成反応器の開発でした。
アンモニア合成触媒に関しては最初にフリッツ・ボッシュが見つけたオスミウム以外に、白金、パラジウム、鉄やイリジウムなどを組み合わせて2500種の触媒を高温高圧下(100~200気圧、300~600℃)で実験を行い、ようやく鉄に促進剤として酸化アルミニウムとカルシウムを加えることでアンモニアの生成量が格段に増加することを見つけ出し、これが純粋な元素より促進剤を重視するという触媒化学の先駆けとなりました。
アンモニアの原料である水素は、高温に加熱したコークスに水を反応させる水性ガス反応で得ていました。ただし、下式に示すように水素だけではなく有毒な一酸化炭素を生成しますので、取扱が難しいという欠点を有していました。
C + H2O = CO + H2 +131.3kJ/mol
これに対してもアンモニアを加えた銅溶液により一酸化炭素を吸収除去出来ることが分かり、アンモニア合成は実現に一歩大きく進みました。この方法はCOSORB法として現在も使用されています。
最後の難問はアンモニア合成反応器の開発でした。高温高圧下で耐えられる材料の探索を進める中で反応器の爆発に幾度も直面したようです。その原因はアンモニアの原料である水素が反応器の材料である鋼組織に侵入し、鋼の炭素と化合するために起きた強度低下でした。今日、この現象は水素脆性として良く知られています。
これに対しても侵入した水素を逃がす構造をカール・ブッシュが考案し、ようやく高温高圧下で耐えることが出来る反応器を実現しました。このような苦労の末、1911年から1912年に掛けてBASF社はパイロットプラントおよび日産2tonの肥料工場を立ち上げることが出来ました。
このように初期のアンモニアプロセスの開発においては、触媒開発とプロセス改善、そして反応器の材料と構造の開発が主題でした。
現在においても触媒によるケミカル合成法の開発が成功するかどうかは、触媒開発と材料、そして反応器の構造開発が大きく命題となっています。
参考資料
- 「大気を変える錬金術、ハーバー、ボッシュと科学の世紀」みすず書房
- 「アンモニア合成」江崎正直
- 現代ドイツ化学企業史 工藤章
アンモニアプロセスの大型化 1970年代に入り第二次世界大戦後の世界的な経済発展とともに、アンモニアプラントの大型化が叫ばれるようになりました。1940年代から1960年にかけてはアンモニアプラントの生産量は日産100~500トンでしたが、1960年代半ばから生産規模は1,000トンを超え、現在では3,000トン規模の建設が主流となっています。
第二次世界対戦前から日本国内でもアンモニアの合成法の研究が始められ、多くの化学会社がハーバー・ボッシュ法以外の技術を開発するために努力を重ねてきました。戦後の1969年に米国ケロッグ法を採用したが日産1,000トンのアンモニアプラントが旧三井東圧(現三井化学)のもとで建設運転された結果、肥料以外に化学基礎原料として需要が増加したアンモニアに対応することが可能となったようです。
この時代のもう一つの変化はエネルギー源の変革でした。それまで石炭が主流であったのが石油にシフトされ、先ほどの1,000トンアンモニアの原料も石油から分離されたナフサでした。その原料変換に伴いガス化技術も大きく変貌し、高活性触媒開発により水蒸気改質法が完成されました。この水蒸気改質触媒は主体がNiでしたが、硫黄化合物などにより被毒されることが知られていました。そこで硫黄化合物を効率的に除去する脱硫触媒が開発されるようになって、初めてNi系水蒸気改質触媒が広く採用されるようになりました。
水蒸気改質反応は吸熱反応で化学平衡的には高温が望ましく、さらに次式で分かるように圧力が低いほど反応が進行します。下記にこの水蒸気改質反応と同時に進行するCO転化反応を示します。このCO転化反応は発熱反応ですが、全体的に吸熱反応となりますので常時外部から加熱する必要があります。
CH4 + H2O = CO + H2 + 206.1kJ/mol
CO + H2O = CO2 + H2 - 41.2kJ/mol
この水蒸気改質触媒の開発とともに触媒を充填する水蒸気改質反応管の材料の開発が進められました。改質管の表面は燃焼ガスからの火炎輻射にさらされるので、表面温度は1000℃近くまで達します。アンモニアプロセスの場合には原料となるガス圧力も高く改質管内圧力も3~4MPaとなるので、高温での強度低下とそれによるクリープ破断の可能性が大きくなり、一般的なステンレス鋼では長時間の運転にはとても耐えきれません。そこで改質管材料の開発が進められ、1970年代には商品名HK-40という20Cr-20Niを主成分とする耐熱合金が発明され、水蒸気改質反応を進めることが出来るようになりました。 アンモニアプロセスの省エネルギー化 水蒸気改質反応は低圧ほど有利ですが、後述するアンモニア合成反応では高圧が有利です。そのために水蒸気改質反応を行うガス化工程とアンモニア合成反応工程の間に圧縮機を設置する必要がありました。プラントの大型化以前では合成ガスの流量も少なく圧縮機の型式も往復動式が採用されていました。しかし大型化を進めるためには往復動式圧縮機では対応出来ずに経済的にも不利でした。そこで大型化に向いた遠心式圧縮機の開発が推し進められるようになり、その結果、プラント規模で1,000トン以上、吐出圧力も30MPaを超える遠心式大型合成ガス圧縮機が登場し、本格的な大型アンモニアプロセスの完成となりました。
1970年代に起きた石油危機はアンモニアプロセスに変革をもたらしました。それがアンモニアプロセスの省エネです。それと同じ時期にアンモニア原料の天然ガス転換が始まりました。
1970年代までのアンモニアプロセスのエネルギー消費量は天然ガスをベースにすれば約40GJ/ton-NH3でした。しかし、プロセスライセンサーとエンジニアリング企業の技術開発の結果、このエネルギー消費量(総合原単位)は2010年代には29GJ/ton-NH3まで改善されました。改善点の主な項目を上げますと、
- 水蒸気改質管材料の開発による水蒸気改質圧力の上昇
- 高活性アンモニア合成触媒の開発による水素ロスの削減
- 合成ガス中のCH4, Arなどの除去システム採用による合成圧力の低下
- 省エネ型二酸化炭素吸収溶液の開発による再生熱の削減
現在、稼働中の多くのアンモニアプラントの生産規模は1,800MTPD~2,200MTPDで、3,300MTPD規模の大型アンモニアプラントも登場しています。これらのアンモニアプラントのほとんどは下記に示すライセンサー4社のプロセスを採用しています。
- Ammonia Casale(スイス)
- Haldor Topsoe(デンマーク)
- KBR(米国)
- Uhde(ドイツ)
その中でも省エネと大型化に実績があるライセンサーはKBRとUhdeの2社で、この両者プロセスを対象としたレポートに依れば、生産規模日産3,300トンで総建設費は約$1,000million(1,200億円)と報告されています。
アンモニアプロセスの概要 1970年代初めからアンモニアプラント業界を席巻してきたのが米国Kelloggのアンモニアプロセスです。このプロセスは天然ガスを原料に合成圧力として15~30MPaを採用しており、「アンモニアプラントの大型化」で説明しましたHK-40を採用した改質管と遠心式大型圧縮機を採用していました。
このKelloggは現在のKellogg Brown & Root (KBR)の前身で、国内では東洋エンジニアリングのアンモニアプロセスのライセンサーでもあります。この“既存のアンモニアプロセス”ではKelloggのアンモニアプロセスを対象に説明していきます。
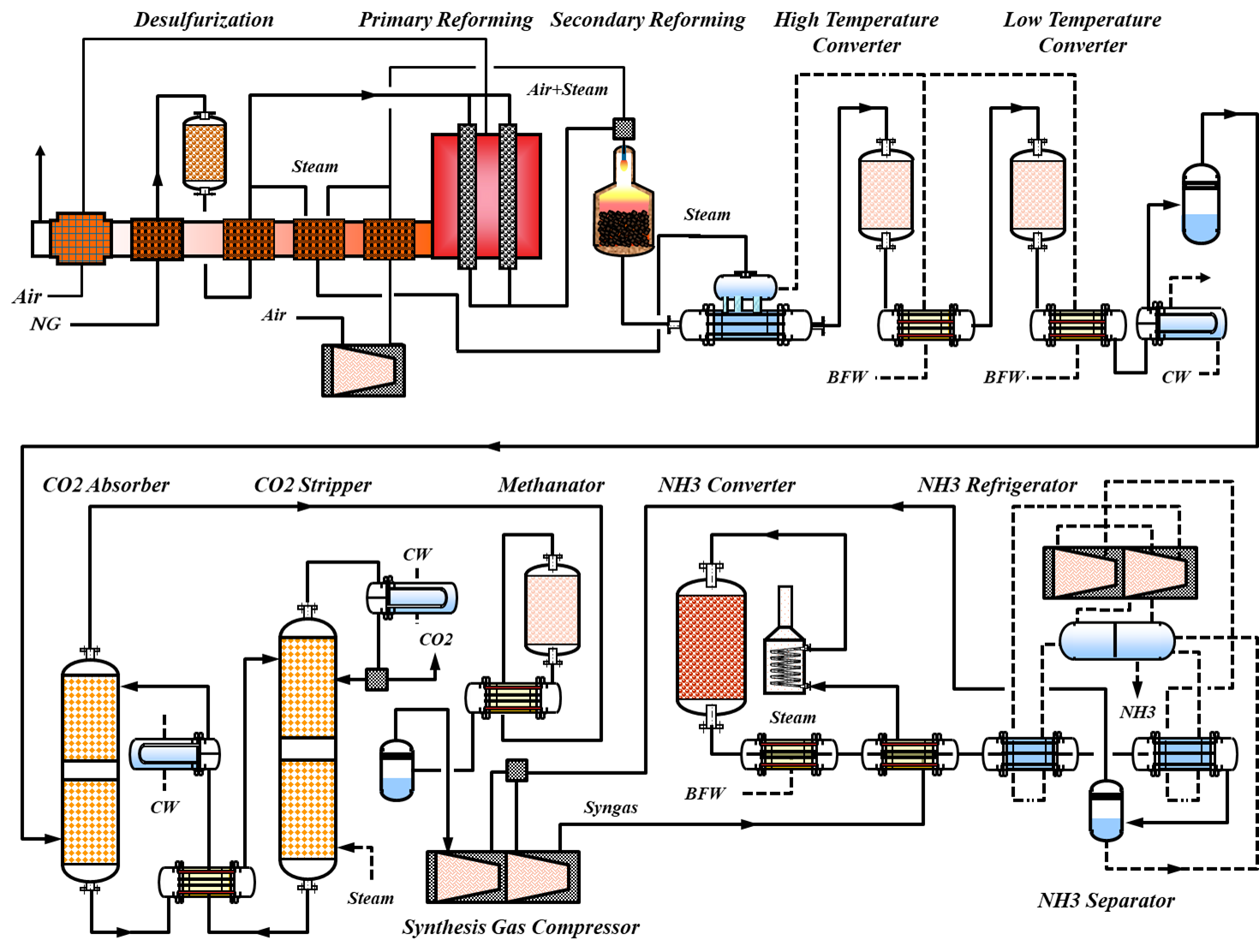
このKelloggプロセスは以下の8つの工程から構成されています。
- 脱硫工程(Desulfurization section)
- 水蒸気改質工程(Primary Reforming section)
- 二次改質工程(Secondary Reforming section)
- CO転化工程(CO Shift section)
- CO2吸収工程(CO2 Removal section)
- メタン化工程(Methanation section)
- 合成ガス圧縮工程(Synthesis Gas Compression section)
- アンモニア合成工程(Ammonia Synthesis section)
- アンモニア冷凍工程(Ammonia Refrigeration section)
上記の工程の関係を次図に示します。以下のおおまかな流れを説明します。
- 原料の天然ガス(CH4が主成分)を脱硫工程に供給し、下流の水蒸気改質触媒などの触媒毒(硫黄化合物など)を除去します。
- その後、水蒸気改質工程において原料天然ガを改質用スチームでH2 & COに改質します。この改質反応は吸熱反応なので天然ガスの一部を燃料として使用します。
- 次の二次改質工程ではアンモニア原料のN2を供給するために空気を供給し、水蒸気改質工程で残存したCH4をさらに改質します。
- 次のCO転化工程でCOを水素に転化させ、アンモニア原料である水素を増量して合成ガスを作ります。
- CO2吸収工程では合成ガス中のCO2を吸収除去します。
- メタン化工程では微量のCO & CO2をCH4に変換して無害化します。
- 圧縮された合成ガスをアンモニア合成工程に供給しアンモニアを合成します。
- アンモニア冷凍工程はアンモニア合成工程での冷媒として使用します。

|



 前のページへ
前のページへ